生体機能医科学研究室
概要
生体の機能は、様々な環境変化に対応できるように発揮されたり調節されたりします。私達は、遺伝情報や蛋白質がどのように調節され機能するかについて、1)神経系の発生・再生の機構、2)遺伝子の発現調節機構、3)細胞骨格因子の構造と機能、といった課題を挙げ、生物学の根本的命題の解明や、医学・医療への展開に向けて追求しています。特に、1)では自らが発見したLOTUSという神経再生促進物質を利用した神経再生医療技術の創成について、2)では遺伝情報の読み出しの仕組みの理解と、その破綻によって起きる疾患(糖尿病、癌など)の克服について、3)では細胞分裂の中心的役割を担う微小管について、力点を置いた研究を展開しています。
准教授 片岡 浩介(かたおか こうすけ) ResearchMap →

<略歴>
東京大学大学院理学系研究科博士課程修了(1994年)理学博士。1994年から東京大学医科学研究所・癌ウイルス研究部・助手。2000年から東京工業大学・フロンティア創造共同研究センター・助手。2003年から奈良先端科学技術大学院大学・バイオサイエンス研究科・准教授。2013より現職(大学院生命医科学研究科准教授)。
<メッセージ>
分子生物学と生化学を基盤に、培養細胞や疾患モデルマウスを駆使して、疾患の分子基盤の解明を目指します。最先端研究を展開しながら、単に実験技術を習得するのではなく、科学的・論理的思考を身につけ、研究計画の立案から実行までを行える総合力のある人材の育成を目指します。また、研究分野以外の道でも大切な文章表現やプレゼンテーション能力の習得・向上にも重点を置きます。
東京大学大学院理学系研究科博士課程修了(1994年)理学博士。1994年から東京大学医科学研究所・癌ウイルス研究部・助手。2000年から東京工業大学・フロンティア創造共同研究センター・助手。2003年から奈良先端科学技術大学院大学・バイオサイエンス研究科・准教授。2013より現職(大学院生命医科学研究科准教授)。
<メッセージ>
分子生物学と生化学を基盤に、培養細胞や疾患モデルマウスを駆使して、疾患の分子基盤の解明を目指します。最先端研究を展開しながら、単に実験技術を習得するのではなく、科学的・論理的思考を身につけ、研究計画の立案から実行までを行える総合力のある人材の育成を目指します。また、研究分野以外の道でも大切な文章表現やプレゼンテーション能力の習得・向上にも重点を置きます。
准教授 林 郁子(はやし いくこ) ResearchMap →

<略歴>
東京大学大学院工学系研究科博士課程修了(1997年)工学博士。1996年より日本学術振興会特別研究員、1997年生物分子工学研究所博士研究員、2000年バーナム研究所(米)博士研究員、2002年トロント大学オンタリオがん研究所(カナダ)博士研究員を経て現職(大学院生命医科学研究科准教授)。
<メッセージ>
細胞分裂・染色体分配の中心的役割を担う微小管関連タンパク質群について研究を行っています。結晶構造解析、生化学、分子生物学、細胞生物学的手法によって、微小管細胞骨格による細胞内ダイナミクスの分子制御メカニズムを解明することを目指しています。
東京大学大学院工学系研究科博士課程修了(1997年)工学博士。1996年より日本学術振興会特別研究員、1997年生物分子工学研究所博士研究員、2000年バーナム研究所(米)博士研究員、2002年トロント大学オンタリオがん研究所(カナダ)博士研究員を経て現職(大学院生命医科学研究科准教授)。
<メッセージ>
細胞分裂・染色体分配の中心的役割を担う微小管関連タンパク質群について研究を行っています。結晶構造解析、生化学、分子生物学、細胞生物学的手法によって、微小管細胞骨格による細胞内ダイナミクスの分子制御メカニズムを解明することを目指しています。
研究内容
1)細胞機能の維持機構とその破綻による疾患の解明(片岡)
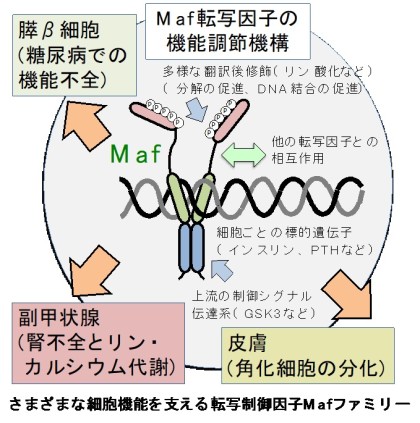
体を構成するさまざまな細胞の機能は、特異的に発現する遺伝子群が支えています。その発現をコントロールするのは、それぞれの細胞で働く転写制御因子です。私達は、膵島β細胞(インスリンを分泌し、血糖値を下げる)の新規転写因子を発見し、MafAと命名しました。MafAは他の転写因子(Pdx1やBeta2)と恊働してβ細胞の機能を支えています。特定の転写因子の組み合わせがiPS細胞を生み出すように、これらの転写因子群はβ細胞を生み出すリプログラミング技術にも応用されています。また2型糖尿病の病態・要因であるβ細胞の機能不全の原因は長年にわたって不明でしたが、MafAの活性調節の仕組みが破綻してMafAの量と機能が低下することが大きな問題であると分かってきました。転写因子の機能の研究は疾患の分子基盤の理解に欠かせません。MafA/膵島β細胞/糖尿病の他に、MafB/副甲状腺/カルシウム代謝疾患などを対象にした研究を展開しています。
2)細胞分裂を司る微小管細胞骨格因子の構造機能解析(林)
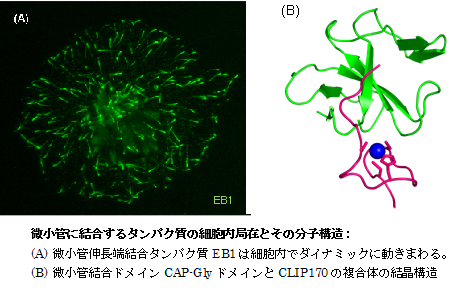
細胞内で線維状構造を形成する細胞骨格因子は細胞の形や強度を保つばかりでなく様々な生体機能の維持にも関与します。なかでも微小管細胞骨格は、染色体分配や細胞移動、小胞輸送にも深く関わり、その機能不全により細胞のがん化がひき起こされます。私達は微小管と細胞小器官とをつなぐ微小管末端集積タンパク質とよばれる分子群に注目して研究を行っています。また原核生物の細胞分裂や遺伝子分配に関わるチューブリン相同タンパク質について、その分子機構を明らかにすることで感染症に対する分子基盤を築くことを目指しています。主な課題は:1)微小管末端結合タンパク質の構造機能解析と微小管反応の生化学的解析。2)植物細胞の形態を制御する表層微小管関連因子の分子間相互作用解析。 3)病原性微生物の毒素遺伝子分配に関わるタンパク質群の構造機能解析。
主要文献(Selected Publications)
‣ Onishi S. and Kataoka K. PIASy is a SUMOylation–independent negative regulator of the insulin transactivator MafA. J.Mol. Endocrinol. 63: 297-308 (2019).
‣ Miyai M., Tsunekage Y., Saito M., Kohno K., Takahashi K., and Kataoka K. Ectopic expression of the transcription factor MafB in basal keratinocytes induces hyper-proliferation and perturbs epidermal homeostasis. Exp. Dermatol. 26: 1039-1045 (2017).
‣ Hayashi I. The C-terminal region of the plasmid partitioning protein TubY is a tetramer that can bind membranes and DNA. J Biol Chem 295: 17770-17780 (2020).
‣ Hayashi I., Oda T., Sato M., and Fuchigami S. Cooperative DNA Binding of the Plasmid Partitioning Protein TubR from the Bacillus cereus pXO1 Plasmid. J Mol Biol 430: 5015-5028 (2018).
‣ Miyai M., Tsunekage Y., Saito M., Kohno K., Takahashi K., and Kataoka K. Ectopic expression of the transcription factor MafB in basal keratinocytes induces hyper-proliferation and perturbs epidermal homeostasis. Exp. Dermatol. 26: 1039-1045 (2017).
‣ Hayashi I. The C-terminal region of the plasmid partitioning protein TubY is a tetramer that can bind membranes and DNA. J Biol Chem 295: 17770-17780 (2020).
‣ Hayashi I., Oda T., Sato M., and Fuchigami S. Cooperative DNA Binding of the Plasmid Partitioning Protein TubR from the Bacillus cereus pXO1 Plasmid. J Mol Biol 430: 5015-5028 (2018).